记者从省食品药品监督管理局获悉,8月16日,国家药品监督管理局批复同意《广东省医疗器械注册人制度试点工作方案》(以下称《方案》),标志着即日起广东省“医疗器械注册人制度”正式落地实施。
《方案》提出,今后广州、深圳、珠海三个试点地区的医疗器械注册申请人可以委托广东省医疗器械生产企业生产产品,允许医疗器械研发机构和科研人员申请医疗器械上市许可,在探索医疗器械产品注册与生产许可“解绑”分离的管理模式上取得突破。
“捆绑制”注册管理不利于研发创新
医疗器械注册人制度,是指符合条件的医疗器械注册申请人可以单独申请医疗器械注册证,然后委托给有资质和生产能力的生产企业生产,从而实现医疗器械产品注册和生产许可的“解绑”。医疗器械注册人制度是现行医疗器械法规背景下的上市许可持有人制度。
近十年来,我国医疗器械创新创业高度活跃,新产品、新业态不断涌现,医疗器械市场规模从2001年到2016年年均复合增长率22.37%,远超全球医疗器械行业7%-8%的增速。
其中,广东的医疗器械产业基础较好,医疗器械创新活跃。据2017年统计数据显示:广东企业获国家食品药品监管总局批准的三类医疗器械155个,约占全国总数1/5;进入总局创新特别审批程序产品数占全国总数1/5;进入总局优先审批程序产品数占全国总数1/3;全省产值约1300亿元,占全国总数的近1/3;向总局报送三类创新51宗,同比增长50%。在新一轮医疗器械行业竞争中,广东面临着更复杂的市场环境、更艰巨的转型挑战,需借助全球配置资源要素,需依靠制度创新促进发展。
2014年6月1日,新修订《医疗器械监督管理条例》及配套规章实施出台。虽然改变了原先由取得生产许可证的企业申办注册的要求,变成先办理产品注册,后办理生产许可,但法规仍要求申请人必须是企业,必须由自己设厂生产产品,注册检验样品不得委托生产,实质上将产品注册与生产许可“捆绑”。
随着我国市场经济体制逐步完善,医药产业创新研发能力不断发展,人民群众对安全、有效和可及药品的需求不断增长的情况下,这种“捆绑制”注册管理的弊端日益凸显,影响了创新研发和持续提高产品质量的责任和热情,限制了创新要素的合理配置,已成为制约我国医疗器械行业进一步发展的因素之一。
2015年8月,国务院印发《关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号)揭开了深化我国药品监管制度改革的大幕。药品、医疗器械上市许可持有人制度是重要内容之一。
2017年10月8日,中共中央办公厅和国务院办公厅联合印发《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,更是明确改革方向,提出加强药品医疗器械全生命周期管理,推动上市许可持有人制度全面实施。及时总结药品上市许可持有人制度试点经验,推动修订药品管理法,力争早日在全国推开。
产品“孵化”期自贸区医疗器械注册申请人即可委托生产
此次《方案》中有关“医疗器械注册人制度”的改革措施主要包括五项。首先,允许中国(广东)自由贸易试验区内的医疗器械注册申请人,以及广州、深圳、珠海市的医疗器械注册申请人可以委托广东省医疗器械生产企业生产样品。这意味着当产品还在“孵化”阶段,就允许自贸区内医疗器械注册申请人委托生产,无论该样品是否进入创新医疗器械特别审批程序。
同时,允许注册人可以自行生产或者委托其他企业生产医疗器械。取得注册证后,注册人具备相应生产能力的,可以在办理医疗器械生产许可后自行生产;注册人不具备相应生产能力的,可以委托其他企业生产,并办理委托生产相关手续。受托人不具备相应生产资质的,可提交注册人的医疗器械注册证办理生产许可。
在销售环节,《方案》提出,注册人可以自行销售医疗器械,无需办理医疗器械经营许可或者备案,也可以委托具备相应条件的医疗器械经营企业销售医疗器械。委托销售医疗器械的,注册人应当对所委托销售的医疗器械质量负责,与受托经营企业签订委托协议,明确双方权利、义务和责任,并加强对受托经营行为的管理,保证其按照法定要求进行销售。
对于现有的已持有注册证的医疗器械生产企业,可以实现注册与生产“剥离”。《方案》提出,省内已取得医疗器械注册证的医疗器械生产企业,可参照《方案》有关规定执行。
此外,鼓励集团公司成为注册人。医疗器械生产企业集团公司可以将各控股子公司的医疗器械注册证集中到集团公司持有。集团公司按各控股子公司生产加工能力将产品进行调配整合,使各子公司成为有特点、有优势、有规模的生产基地,集团公司对各子公司实行统一的质量管理体系,集团公司对所有上市的产品质量负全部责任。
据省食药监负责人介绍,此次《方案》中的试点改革将有利于强化注册人全生命周期责任,鼓励创新研发和持续改进质量,进一步促进科研人才、研发机构和创新企业集聚,优化创新资源的市场配置,加快医疗器械上市。同时,有利于完善医疗器械注册生产监管制度,促进审评标准提升和审评统一,建立有效的跨区域事中事后监管方式。
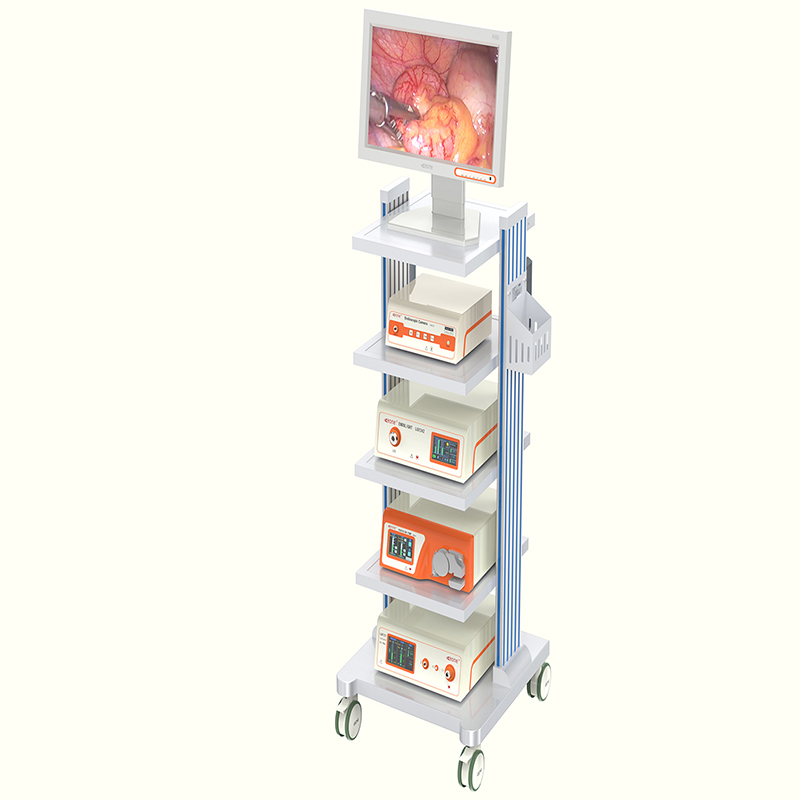
南京利昂医疗设备制造有限公司主要经营U臂DR、悬吊DR、气腹机、DR显示器、膨腔泵、内窥镜摄像机、医用冷光源等医疗器械产品,如有需要,欢迎热线咨询400-025-6776(静音平板DR)或400-025-6806(内窥镜设备)。